NK細胞治療實體瘤新策略,抗體—NK細胞偶聯臨床試驗
ACE1702是一種自然殺傷細胞(NK細胞)療法,正在開發用於治療表達HER2的實體瘤。第一位患者在德克薩斯州休斯頓的安德森癌症中心接受給藥。這項研究將評估ACE1702對不能接受手術或其他治療方案的晚期或轉移性HER2表達的實體瘤患者的安全性、耐受性、藥效學和初步療效。該研究預計將在美國多個主要的腫瘤學基地招募12至24名患者。
Acepodia研發部高級副總裁Mark Gilbert博士表示:“第一位患者接受ACE1702治療後,沒有發生任何不良事件,包括移植物抗宿主病或細胞因數釋放綜合征。我們期待著在臨床上推廣ACE1702,並探索我們獨特的細胞療法治療實體瘤的潛力。”
抗體—NK細胞偶聯
ACE1702是利用Acepodia的ACC技術開發的同種異體現成NK細胞療法,可將腫瘤靶向抗體直接連接到其專有NK(oNK)細胞系表面,具有高水準的啟動受體和低水準的抑制受體,以最大限度地提高腫瘤的殺傷能力。在臨床前研究中,ACE1702在GLP毒理學研究中顯示出良好的安全性,並在體外和體內增強了對HER2 IHC 1+、2+和3+人癌細胞的腫瘤導向細胞毒性。鑒於其強大的功能以及按需快速擴大生產的便利性,ACE1702可能會影響實體瘤的治療方式,因為它的效力和很容易根據需求迅速擴大生產。
“這項試驗的啟動對我們公司來說是一個重要的里程碑,標誌著利用Acepodia專有的ACC技術產生的同種異體NK細胞療法的首次臨床研究。”Acepodia首席執行官Sonny Xiao博士說,“ACE1702利用我們強大的自然殺傷細胞系oNK,並利用我們的ACC平臺增強其抗腫瘤活性,從而形成一種現成的治療方法,我們相信這種療法有可能有效對抗實體瘤。重要的是,我們的同種異體療法可以大規模生產,這最終可以使患者獲得挽救生命的機會。”
關於Acepodia
Acepodia是一家美國和臺灣的私營生物技術公司,通過靈活和綜合的生物設計方法重塑細胞治療領域,主要專注於腫瘤學。該公司的平臺植根於其專有的現成自然殺傷(oNK)細胞系,該細胞系因其強大的抗腫瘤活性而被選中。Acepodia的藥物開發平臺旨在通過嵌合抗原受體技術以及其獨特的ACC(抗體細胞結合)技術來增強oNK細胞的腫瘤親和力,該技術將腫瘤靶向抗體與oNK細胞的表面蛋白連接起來。
ACC技術使用活細胞相容化學,將任何腫瘤靶向抗體連接到人體免疫細胞表面,如Velcro®。這一強大的新的細胞治療發展方法有可能通過釋放多種受體信號通路,顯著提高oNK細胞識別和參與腫瘤的能力。這有可能使acconk療法克服那些阻礙細胞療法有效靶向實體瘤的挑戰。

▲ACC技術平臺作用機制示意圖(圖片來源:公司官網)
除了ACC所賦予的效力優勢外,它的簡單性和模組化、“隨插即用”的特性可以使患者更容易使用細胞治療,並擴展到腫瘤學以外的其他適應症和NK細胞以外的其他細胞系。
2020年7月15日,Acepodia與藥明巨諾達成專屬優先授權合作協定,藥明巨諾獲得Acepodia旗下兩款細胞免疫療法候選藥ACE1702和ACE1655在中國大陸、香港和澳門地區的在臨床和商業化的專屬優先授權。據介紹,這兩款在研產品將分別被開發用於實體瘤和血液系統惡性腫瘤的治療。根據合作協定,Acepodia公司將獲得簽約授權金、階段性付款,以及銷售權利金,具體金額未披露。
基於NK細胞的“現成”策略
NK細胞是人體先天免疫系統的一部分,能對身體內遇到的各種病原體迅速作出反應,是抵禦危險感染或異常細胞的第一道防線,是身體對抗癌症的正常儲備。
它與獲得性免疫系統中的細胞毒性T細胞,扮演著相近的角色。但它們之間不同的是:通常情況下,細胞毒性T細胞需要檢測到病毒細胞表面的MHC,才會引起細胞因數的釋放,進而導致靶細胞裂解或凋亡;而NK細胞可以在沒有抗體或MHC的情況下,識別這些細胞並進行快速的免疫回應。對於那些失去自身標記的MHC-I型的細胞,NK細胞不經過啟動就可以進行殺傷。而這些細胞通常是有害但不能被其他免疫細胞發現並消滅的。
NK細胞因不同於T細胞的非特異性識靶及殺傷機制吸引科學家的探索與開發,以彌補現有的自體細胞療法的局限性。在開發現成的NK細胞療法領域中,Fate Therapeutics和NantKwest是其中的佼佼者。
iPSC衍生的CAR-NK預計於2020年初開始首次人體臨床試驗
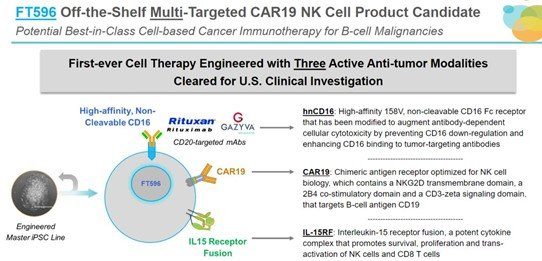
2019年9月,美國FDA批准Fate Therapeutics公司首個具有三種抗腫瘤模式的現成CAR-NK細胞療法(FT596)的IND申請。FT596在不到一年的時間裡被FDA批准進行臨床研究,Fate公司還計畫啟動FT596單藥及聯合CD20單抗治療B細胞淋巴瘤和慢性淋巴細胞白血病的臨床研究。
▲ 圖片來源:Fate
FT596源自iPSC細胞系,其獨特的設計旨在克服CD19抗原逃逸,除了有靶向CD19的專有CAR以外,它還表達了一種新型的高親和力、不可裂解的CD16(hnCD16) Fc受體,該受體已被修飾以增強抗體依賴性細胞的細胞毒性(ADCC),從而能夠同時靶向CD19和其他腫瘤相關抗原,例如CD20。FT596還表達白介素15受體融合蛋白(IL-15RF),這是一種有效的細胞因數複合物,無需系統性細胞因數支持,即可促進NK細胞和CD8 T細胞的存活、增殖和反式啟動。
在ASH上發表的新的臨床前資料表明,作為單一療法施用的FT596表現出持久的腫瘤清除能力和延長的體內存活率。另外,當與靶向CD20的利妥昔單抗聯合使用時,與單獨使用利妥昔單抗相比,FT596在體內顯示出對CD20 +淋巴瘤細胞殺傷的增強。這些資料證實了先前提出的體外研究結果,即FT596獨特的多抗原靶向能力以及候選產品有效克服CD19抗原逃逸的潛力。
FT500 & FT516:首個現成的、iPSC衍生的NK細胞療法正處於I期臨床
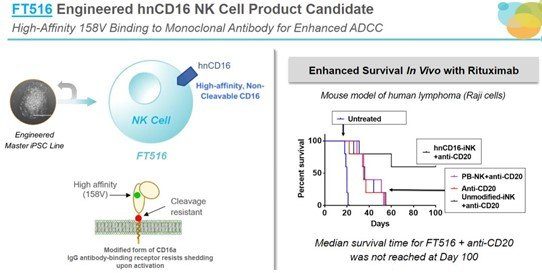
在ASH年會上,Fate公司公佈了兩款NK細胞療法FT500和FT516的I期臨床試驗結果。FT500是iPSC衍生的NK細胞療法,FT516在FT500的基礎上在細胞表面表達了不可裂解的CD16 Fc受體,從而優化了ADCC。
▲ 圖片來源:Fate
該公司的新聞稿指出,FT500是有史以來第一個在美國獲批臨床的源自克隆主iPSC系的細胞療法。初步試驗結果表明,接受FT500治療的前12名晚期實體瘤患者未報告劑量限制毒性和與FT500相關的嚴重不良事件,也未報告細胞因數釋放綜合征、神經毒性或移植物抗宿主病。
FT516正在I期臨床試驗中作為治療急性髓細胞白血病(AML)的單一療法,以及與利妥昔單抗聯合治療晚期B細胞淋巴瘤,是對克隆主工程化iPSC系細胞產品的首次臨床研究。迄今為止,已有2名患者接受了FT516的治療,即將進行正式的反應評估。
NantKwest
2019年6月25日,NantKwest公司的PD-L1 t-haNK新藥臨床試驗申請(IND)獲得美國FDA批准,這是該專案在局部晚期或轉移性實體瘤中的首次人體臨床試驗。2019年12月2日,該公司宣佈在QUILT-3.064試驗的前六名患者中獲得了令人鼓舞的安全性資料。這項首次人體試驗(first-in-human)評估了該公司全球首創(First-in-class) PD-L1 t-haNK細胞療法的安全性和初步療效。
在2020年1月舉行的第38屆JP Morgan醫療健康大會上,黃馨祥博士帶著“登月計畫”的患者的臨床資料,展示了PD-L1.t-haNK聯合N-803療法在一例轉移性胰腺癌中完全緩解。受此影響,NantKwest的股價收盤上漲91%,至6.80美元,是自2015年股票開始交易以來的最大漲幅
基於NantKwest公司的t-haNK平臺的PD-L1 t-haNK細胞療法旨在通過使用CAR結構體提供精確的腫瘤細胞特異性,該結構體利用PD-L1特異性scFv(單鏈抗體片段)設計到該公司專有的haNK細胞中以調節抗體依賴性細胞毒性(ADCC)。PD-L1 t-haNK細胞來自人類衍生的同種異體NK細胞系,經過工程設計以表達靶向PD-L1的CAR,其起源於NantKwest專有的NK-92(aNK)主細胞庫。除了靶向PD-L1,PD-L1.t-haNK還被工程化表達CD16受體(V158 FcγRIIIa)的高親和力變體,是首次設計的,GMP級的,冷凍保存的,現成的雙突變NK細胞療法。
除此之外,還有一些企業和機構都在致力於這類現成的NK細胞療法的開發。日前,來自MD安德森癌症中心一項多中心I/II期臨床試驗(NCT03056339)的研究結果發表在《新英格蘭醫學雜誌》上,來源於臍帶血的CAR-NK細胞在復發或難治性CD19陽性NHL和CLL患者中誘導了高應答率,且未出現重大毒副作用。
結語
NK細胞因其獨特機制在腫瘤免疫療法中取得了亮眼的成績,但現在基於NK細胞的研究大多處於早期研發階段,我們期待早日有療效的NK細胞藥物上市,造福患者!
參考資料:
1.https://www.biospace.com/article/releases/acepodia-initiates-a-phase-1-clinical-trial-evaluating-allogeneic-nk-cell-therapy-ace1702-for-treatment-of-solid-tumors/
