Nature揭秘抗癌細胞療法——129個靶點!
Nature揭秘抗癌細胞療法——129個靶點!
儘管嵌合抗原受體(CAR)的療法(以下簡稱CAR療法)安全性和有效性的臨床試驗數量在全球迅速增加,但一直未有對CAR設計、靶點等信息的全面分析。

1月6日,最新發表在Nature Biotechnology上的一項分析報告中[1],來自美國威爾康奈爾醫學院、中國醫學科學院腫瘤醫院深圳醫院等機構的研究團隊構建了CAR療法(CAR- T、CAR-NK等)的臨床試驗數據庫,該數據庫涉及來自20個國家的500多項臨床試驗、2萬多例患者。
通過與轉錄和蛋白質數據相結合,科學家們獲得了一個可用於CAR細胞療法的“靶點圖譜”,包括100多個靶點。
以下摘編該報告中的部分數據:
數據①:2014-2018年,臨床試驗數量增加4倍
近年來,CAR療法臨床試驗的數量和類型都迅速增加。從2014年到2018年,CAR工程細胞療法在全球啟動的臨床試驗數量增加了4倍(圖1),這反應了業界對這類療法以及Immuno-Oncology的熱情投入。


1)80%以上試驗在中國和美國執行中
總體來說,納入分析的501項CAR細胞療法抗癌臨床試驗中,>80%在中國和美國執行中(圖1a),大部分試驗處於I或I/II期 (圖1b),並正在積極招募中(圖1c)。
2)T細胞是最主要的工程細胞來源
大部分(96.4%)的CAR療法臨床試驗以T細胞作為工程細胞來源(圖1k)。
3)4-1BB是最常見的共同刺激區

CAR的設計經歷了幾次迭代。所有CAR都包含一個負責結合抗原的胞外區,而胞外區連接著中間鉸鏈區、跨膜區以及胞內信號區(圖1h)。第一代、第二代和第三代CAR之間的差異取決於它們所包含的共同刺激區的數量(分別為0個、1個和2個)[2]。報告顯示,被報導最多的共同刺激區是4-1BB,其它常被用到的共同刺激區包括CD28、CD27、OX40(圖1i)。第四代CAR的差異在於其通過進一步的基因工程改造招集其它免疫細胞的能力。
數據②:64個進入臨床試驗的CAR靶點
靶點選擇是CAR設計最重要的部分之一。為了增加可被CAR療法治療的病患數量,業界正在積極分析多種靶點的安全性和抗癌能力,下圖匯總了64個正在臨床研究中被分析的CAR靶點。
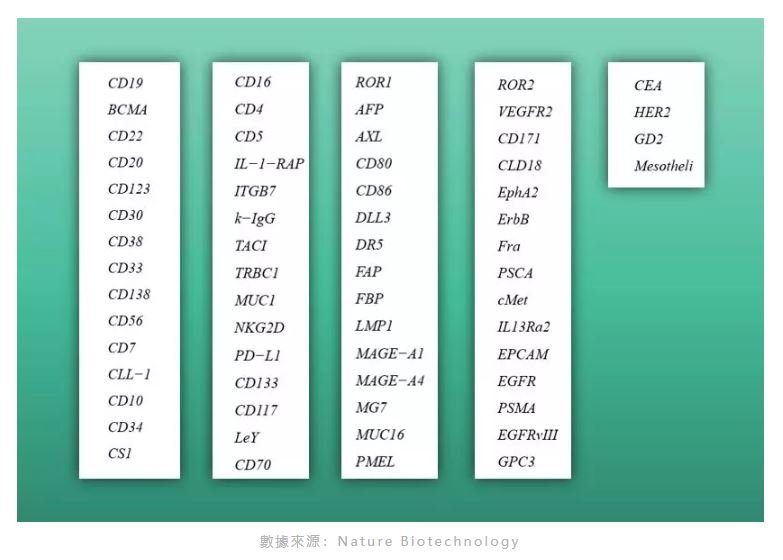
1)8個靶點被用於同時對抗實體瘤和liquid cancer
以上64個靶點中,23個靶點僅被用於對抗liquid cancer,33個靶點僅被用於對抗實體瘤,8個靶點被用於同時對抗實體瘤和liquid cancer,包括MUC1、NKG2D 、PD−L1、CD133、CD117、LeY、CD70、ROR1(圖2a)。

2)對抗liquid cancer最常用的靶點
CD19、BCMA和CD22是對抗liquid cancer的CAR療法最常用的靶點。
3)對抗實體瘤最常用的靶點
Mesothelin、disialoganglioside(GD2)、HER2、carcino embryonic antigen (CEA)、glypican 3 (GPC3)、EGF receptor variant III (EGFRvIII)是對抗實體瘤的CAR療法最常用的靶點。
4)六大常見癌症適應症
淋巴瘤、白血病(淋巴細胞和髓細胞)、骨髓瘤、胰腺癌、肝癌和神經母細胞瘤所涉及的臨床試驗最多(圖2b)
數據③:CAR靶點在正常組織和癌症組織中的表達分析
大多數目前在臨床研究中的CAR靶點是在正常細胞和組織中也會表達的抗原,理論上,這就存在“off-tumor targeting”以及產生毒性的風險。該報告發現,與預期一樣,被用於大部分臨床試驗的CAR靶點在正常組織中低表達,但CD123和MUC1是兩個例外。

為了更好地理解哪些癌症類型更適合利用CAR療法治療,科學家們還分析了CAR靶點在癌症組織中的表達模式。他們發現,CD19在大多數淋巴瘤樣本中均有中-高(M–H)表達。此外,α-fetoprotein(AFP)是最值得注意的靶點之一,該蛋白在所有HPA肝癌樣本中均有表達,且主要是中-高(M–H)表達,並有證據表明,相對正常組織,AFP在肝癌中過量表達(圖3c)。
數據④:65個潛力CAR靶點
該報告還提出了65個未進入臨床研究的潛在CAR靶點,具體如下:

這些靶點中有8個已被FDA批准用於其它療法,分別為GLRB、KCNN4、ALPPL2、SLC22A12、HMMR、CD2、CD3G和CD3D (圖4g)。此外,TNFRSF13C和CD37最近已被作為CAR靶點在臨床前模型中進行測試。

總結來說,報告作者們認為,這項分析可幫助CAR療法的設計(圖5),改善靶點與患者的匹配,真正發揮CAR療法(CAR-T、CAR-NK等)的抗癌潛能,使更多患者獲益。



