今日分享一則胎盤間充質幹細胞治療膝骨關節炎相關的臨床文獻。這項臨床試驗的原材料是冷凍保存的人胎盤間充質幹細胞,共納入26名II-III期膝骨關節炎患者。結果顯示,三次關節內注射低溫保存的胎盤間充質幹細胞聯合透明質酸治療膝骨關節炎是安全有效的,患者關節疼痛、僵硬及功能障礙得到顯著改善,並在1年隨訪中提供持續的臨床改善。
在醫學領域,膝骨關節炎(Knee Osteoarthritis, KOA)作為一種常見的退行性關節疾病,長期困擾著數以億計的患者。
隨著人口老齡化的加劇和肥胖率的上升,KOA的發病率逐年攀升,傳統治療方法如藥物治療、物理治療及手術治療雖能在一定程度上緩解症狀,但往往難以根治,且存在副作用大、療效有限等問題。
近年來,幹細胞療法作為一種新興的治療手段,為KOA患者帶來了新的希望。

最近,發表在“ BMC Musculoskeletal Disorders”上的一篇名為“Effectiveness and safety of multiple injections of human placenta-derived MSCs for knee osteoarthritis: a nonrandomized phase I trial”的臨床試驗表明,三次關節內注射低溫保存的胎盤間充質幹細胞聯合透明質酸治療膝骨關節炎是安全有效的,並在1年隨訪中提供持續的臨床改善 [1]。
26名患者臨床實踐:
冷凍保存的胎盤間充質幹細胞,顯著改善膝骨關節炎
這項臨床試驗的原材料是冷凍保存的人胎盤間充質幹細胞(hP-MSCs)。
該研究採用非隨機化、開放標籤設計,共納入26名II-III期KOA患者,分為對照組(僅接受透明質酸治療)和MSC組(接受透明質酸聯合hP-MSCs治療)。
經過三次關節腔內注射(每次間隔4周),並對患者進行為期1年的隨訪觀察。
研究結果顯示:
1.安全性良好:首先是安全性問題,在治療過程中實驗組並未觀察到嚴重不良反應,僅部分患者出現輕度疼痛、腫脹等短暫不適,且均在數日內自行緩解。
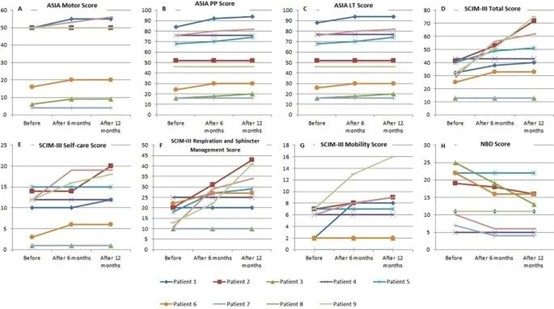
2.療效顯著:其次是治療效果,與對照組相比,MSC組患者在6個月和1年時的WOMAC評分和VAS評分顯著降低,表明關節疼痛、僵硬及功能障礙得到顯著改善。
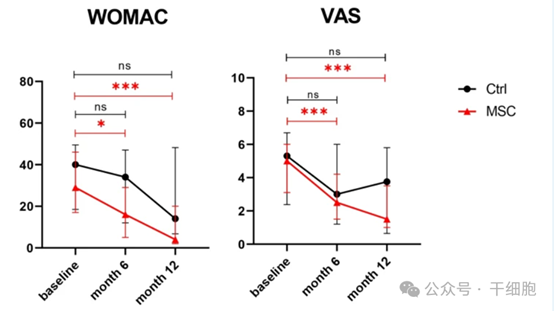
(圖片來自參考文獻1)
- 機制探索:再者是相關的機制學探索,如下圖所示,血清學分析顯示,MSC組患者血清中IL-2水準顯著降低,提示胎盤間充質幹細胞具有顯著的抗炎作用。
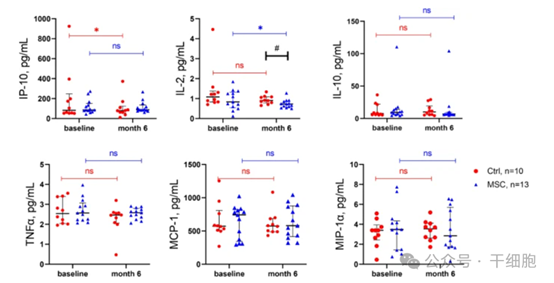
(圖片來自參考文獻1)
然而,MRI分析未發現兩組患者在軟骨厚度和光學密度指數上的顯著差異,這可能與治療時間較短或樣本量較小有關。
多項臨床證實:幹細胞治療骨關節炎具有多重益處
無獨有偶,此前,發表在“Journal of Experimental Orthopaedics”上的一篇名為“Stem cells for the treatment of early to moderate osteoarthritis of the knee: a systematic review”的綜述就也總結了近些年來幹細胞療法在OA上的臨床益處。

(圖片來源於參考文獻3)
- 疼痛緩解方面
大多數研究中研究者們都使用VAS評分進行疼痛緩解的評估,另外有六項臨床研究使用了骨關節炎指數(WOMAC)進行疼痛緩解的評分。
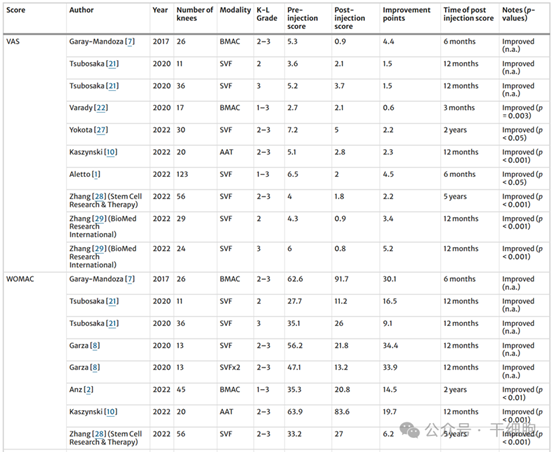
(圖片來源於參考文獻3)
由以上的結果我們不難看出,經過3個月~5年時間不等的隨訪,經由幹細胞注射後患者的疼痛評分大部分都有著顯著下降,改善幅度在0.9至5.2分之間,這意味著患者的疼痛得到了顯著的緩解。
2.功能改善方面
在評判臨床治療OA療效方面,除了對於疼痛的緩解之外,機體功能的改善也是很重要的一點,膝關節功能的改善是衡量治療效果的重要指標。
研究者匯總了近6年來的研究資料,主要結果如下圖所示,研究者主要採用了膝關節損傷和骨關節炎結局評分(K.O.O.S.)、膝關節臨床功能評分(K.S.S.)、EQ-5D-5L問卷和影像學分析等資料來對膝關節功能改善做出較為客觀的分析。
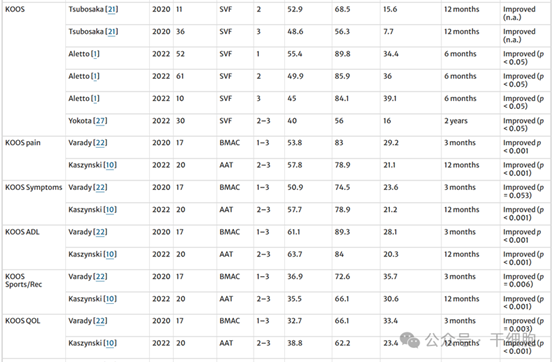
(圖片來源於參考文獻3)
結果顯示,經過幹細胞治療後,患者的膝關節功能評分顯著提升,膝關節的內翻機械軸從1.5°提高到1.8°,骨髓病變大小從123.5 mm^2減小到90.3 mm^2,而用於檢查軟骨修復的MOCART評分也從46.5提高到57.1,以上證據都表明幹細胞療法治療後患者膝關節的靈活性和活動能力都得到了不同程度的改善。
3.安全性良好
研究者匯總了12篇文獻,共統計了539名OA患者,其中有4例患者注射完幹細胞之後出現注射部位周圍疼痛,抽吸部位輕微出血的症狀,僅有2例患者出現了注射部位周圍輕微發紅或腫脹的症狀。從以上結果可以看出,幹細胞治療的安全性較高,且沒有發現嚴重的不良反應。
間充質幹細胞改善膝骨關節炎的優勢
膝骨關節炎是一種以關節軟骨退化、軟骨下骨異常為特徵的慢性疾病,主要表現為關節疼痛、僵硬、腫脹及活動受限。
據統計,全球約有5.28億人受此病困擾,且隨著年齡的增長,患病率還在顯著上升。傳統治療方法如非甾體抗炎藥、糖皮質激素注射及關節置換術等,雖能暫時緩解症狀,但長期效果有限,且可能帶來一系列副作用,如胃腸道不適、感染風險增加等。
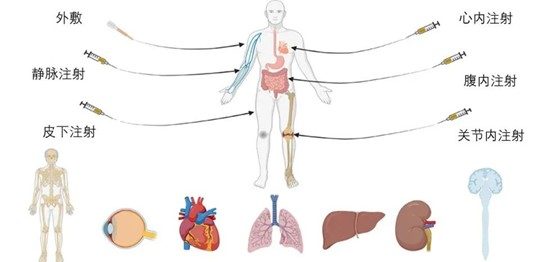
幹細胞療法,特別是間充質幹細胞的應用,為KOA的治療開闢了新的途徑。
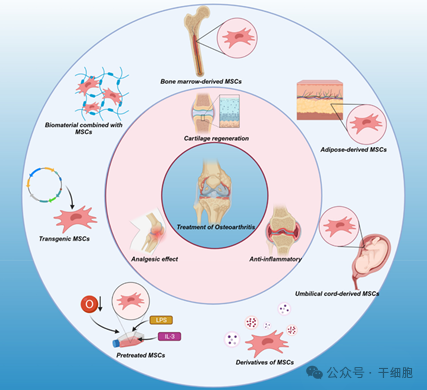
(圖片可見參考文獻2)
如上圖所示,MSCs具有多向分化潛能,能夠分化為軟骨細胞、成骨細胞等,可以直接參與受損關節組織的修復與再生。此外,MSCs還具有免疫調節和抗炎作用,能夠減輕關節炎症,改善關節微環境,從而促進軟骨修復。
與傳統治療方法相比,幹細胞療法具有以下顯著優勢:
1.精准修復:MSCs能夠定向遷移至受損部位,通過分化為軟骨細胞直接參與軟骨修復,提高治療效果。
2.抗炎作用:MSCs通過分泌多種抗炎因數,減輕關節炎症,緩解疼痛,改善關節功能。
3.安全性高:幹細胞療法採用自體或異體幹細胞,來源廣泛,且經過嚴格篩選與培養,確保治療的安全性。
小結
近年來,幹細胞為膝骨關節炎帶來了全新的選擇。未來,仍需開展更多的研究來推動其更為廣泛的臨床應用,比如,幹細胞來源、製備工藝及品質控制需進一步優化,以確保治療的安全性和有效性。其次,仍需大規模、多中心、隨機對照試驗進行長期療效的進一步探討。
隨著科學技術的不斷進步和臨床研究的深入,幹細胞改善膝骨關節炎更多高品質的研究成果有望湧現,為膝骨關節炎帶來更加安全、有效的改善方案。
参考文献:
[1]Holiuk, Y., Birsa, R., Bukreieva, T. et al. Effectiveness and safety of multiple injections of human placenta-derived MSCs for knee osteoarthritis: a nonrandomized phase I trial. BMC Musculoskelet Disord 26, 418 (2025).
https://link.springer.com/article/10.1186/s12891-025-08664-2#Abs1
[2]Chen Y, Cheng RJ, Wu Y, Huang D, Li Y, Liu Y. Advances in Stem Cell-Based Therapies in the Treatment of Osteoarthritis. Int J Mol Sci. 2023 Dec 28;25(1):394. doi: 10.3390/ijms25010394. PMID: 38203565; PMCID: PMC10779279.