“武”“伊”高強 | 肝癌免疫聯合療法客觀緩解率達31%
近期,2019年美國臨床腫瘤學會(ASCO)年會上公佈了1/2期CheckMate 040 臨床研究中納武利尤單抗聯合伊匹木單抗用於既往接受過索拉非尼治療的晚期肝細胞癌患者(HCC)的首個臨床研究結果。此次研究結果首次證實了免疫聯合治療方案在晚期肝細胞癌患者中兼具療效與安全性。
① 客觀緩解率(ORR)達31%,中位緩解持續時間(mDoR)為17.5個月;
② 最長中位總生存期(mOS)達22.8個月,30個月總生存率高達44%;
③ 無論PD-L1表達水平如何,所有治療組均觀察到客觀緩解。
一馬當先
CheckMate 040引領肝癌免疫治療風向標
CheckMate 040是一項正在進行中的開放標籤、多隊列、1/2期臨床研究,旨在評估納武利尤單抗或者以納武利尤單抗為基礎的聯合治療方案對晚期肝細胞癌患者的療效與安全性。該研究共包含6個隊列。其中,隊列1和隊列2是納武利尤單抗的劑量爬坡與劑量擴展試驗。這兩項隊列的試驗結果表明,納武利尤單抗單藥治療不同疾病原因、不同階段、不同地區的晚期肝癌患者,均有鼓舞人心的表现[1,2,3]:
1
生存獲益提升:未接受索拉非尼治療的一線客觀緩解率(ORR)為20-23%,接受過索拉非尼治療的二線ORR為16-19%。且緩解率的提高可轉化為患者的生存獲益,一線初治患者中位總生存期(mOS)高達28.6個月,二線經治患者mOS分別為15.6個月(擴展組)和15個月(遞增組)[1]。一線初治和二線經治的一年生存率分別為73%和60%[2]。
2
東西方人群療效近似:在入組的二線患者中,包括中國人在內的亞洲患者佔入組總人數的近50%。其中,總人群和亞洲人群的24個月生存率分別為33.6%和34.5% ,顯示了亞洲患者的療效和全球患者的療效幾乎沒有差別[3]。
3
HBV與HCV感染患者均能獲益:亞洲人群中,HBV與HCV感染患者mOS均為14.8月。 34%的HBV感染患者生存超過2年,無異於總體療效[3]。這一結果對中國患者意義重大,因為在中國的肝癌患者中,乙肝病毒感染的比例較大。
4
安全性良好:納武利尤單抗的安全性與其在其他瘤種觀察到的結果幾乎一致,沒有新的安全性問題。治療相關的不良事件多為1-2級,3-4級不良反應較少,且可逆可控[1]。
基於以上結果,CheckMate 040研究無疑為PD-1抑製劑治療晚期肝細胞癌注入了信心。在PD-1 抑製劑被國內外指南廣泛推薦作為晚期肝癌二線治療方案的背景下,納武利尤單抗基於其在CheckMate 040研究中的一線數據,還被2018年歐洲腫瘤內科學會(ESMO)肝細胞癌的診斷、治療和隨訪指南唯一推薦用於肝細胞癌的一線治療。

IO+IO
免疫聯合治療證實療效,客觀緩解率達31%
此次在ASCO大會上發布的隊列4,是CheckMate 040未講完的故事。該列隊探索性地評估了三種不同劑量的納武利尤單抗和伊匹木單抗聯合給藥方案的安全性和有效性[4](圖1):

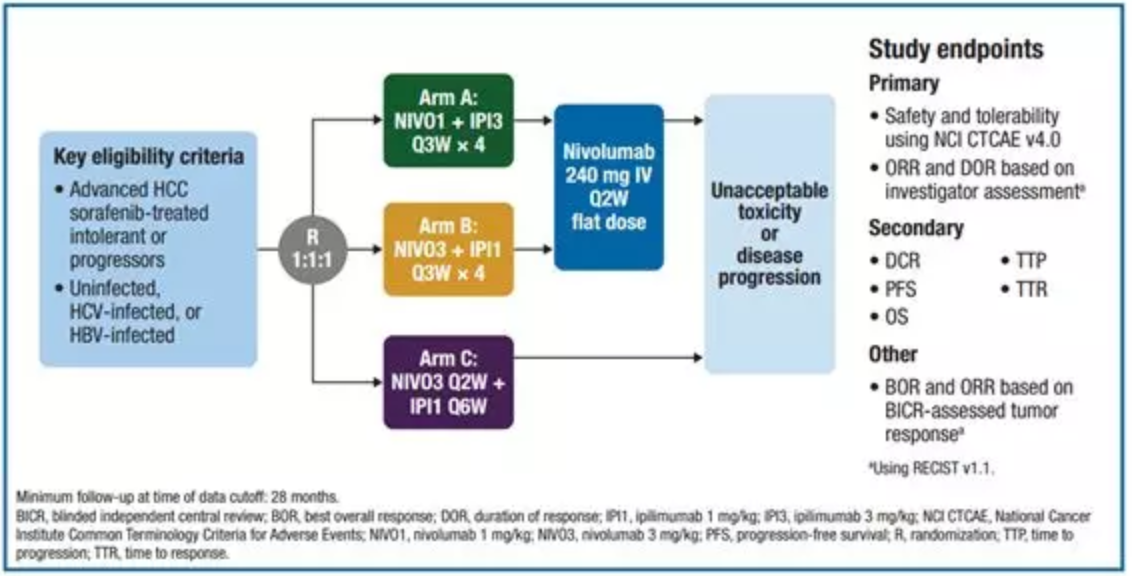
圖1 CheckMate 040隊列4臨床試驗設計
該研究結果首次證實納武利尤單抗聯合伊匹木單抗在晚期肝癌中療效顯著且安全性可控:
1
客觀緩解率達31%:經過至少28個月的隨訪,由盲法獨立中心審查委員會(BICR)根據實體瘤評價標準1.1版(RECIST v 1.1)評估的客觀緩解率(ORR)為31%。其中,A組,B組和C組的疾病控制率(DCR)分別為54%,43%和49%(如圖2、圖3所示)。
2
中位緩解持續時間達17.5個月:至數據截止時,DoR為17.5個月,其中有7例完全緩解(CR),A組中有4例CR(如圖3所示)。

圖2 CheckMate 040隊列4各組療效瀑布圖

圖3 CheckMate 040隊列4療效評估結果
3
最長中位總生存期(OS)達22.8個月:A組、B組和C組的中位總生存時間(mOS)分別為22.8個月、12.5個月和12.7個月,24個月總生存(OS)率分別為48%、30%和42%。其中,A組患者(即納武利尤單抗1 mg/kg聯合伊匹木單抗3 mg/kg治療,每3週1次,連續用藥4個週期後,序貫納武利尤單抗240 mg ,每2週1次)的中位OS最長,達到22.8個月;30個月OS率高達44%。

圖4 CheckMate 040隊列4各組OS結果
4
無論PD-L1表達水平如何,所有治療組患者中均觀察到臨床獲益:在全部隊列患者中,5%獲得完全緩解,26%獲得部分緩解。且無論PD-L1表達水平如何,均觀察到客觀緩解(如圖5所示)。
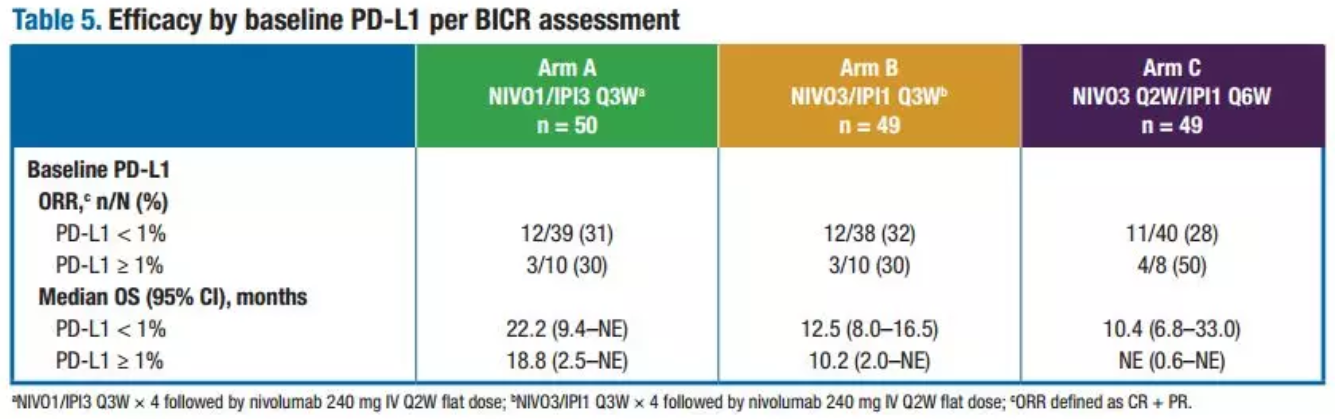
圖5 CheckMate 040隊列4不同PD-L1表達水平亞組療效評估結果
5
安全性可控,沒有新增的不良反應:各治療組中,A組、B組和C組的治療相關不良事件(TRAEs)發生率分別為94%、71%和79%。最常見的3-4級TRAEs包括瘙癢、皮疹、腹瀉、穀草轉氨酶升高和脂肪酶升高。整體屬於可防可控範圍內。免疫聯合治療方案顯示出可接受的安全性,在所有治療組中,均未觀察到因增加伊匹木單抗而出現的新的不良反應。
作為肝癌免疫治療領域的關鍵研究,CheckMate 040研究設計的全面性不僅體現在納入了不同疾病原因、不同階段、不同地區的肝癌患者,其隊列5還將預後較差的Child-Pugh B級晚期HCC患者未盡需求考慮在內。該研究中入組了49例Child-Pugh B級患者,包括既往接受或未接受過索拉非尼治療的患者,以及HBV或HCV感染和非感染人群。試驗結果證明,納武利尤單抗在各個亞組均觀察到持久的療效和安全性。其中,研究者評估的總體人群ORR和DCR分別達12.2%和55.1%,中位OS達7.6個月[5],而既往研究中此類患者接受索拉非尼治療的OS僅為4個月左右[6-8]。
![]()
回顧免疫療法在肝癌治療中的發展歷程,CheckMate 040無疑具有里程碑式的意義,其豐富的臨床研究結果奠定了免疫腫瘤藥物治療在肝癌系統性治療中的地位。在肝癌未來的發展趨勢中,除了免疫聯合治療,更多關於免疫治療與大分子靶向藥物、小分子靶向藥物、化療、消融介入、手術聯合治療的研究進展與應用也令人期待。
注:
1.納武利尤單抗(歐狄沃®,nivolumab)在中國大陸僅獲批用於治療表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、既往接受過含鉑方案化療後疾病進展或不可耐受的局部晚期或轉移性非小細胞肺癌(NSCLC)成人患者;
2.伊匹木單抗(ipilimumab)尚未在中國大陸獲批上市;
3.截至目前,尚無免疫腫瘤治療藥物在中國大陸獲批肝癌適應症。
文章出自:醫世象 https://mp.weixin.qq.com/s/ZeUG0xHjCxFQAhxiM7z6mg
