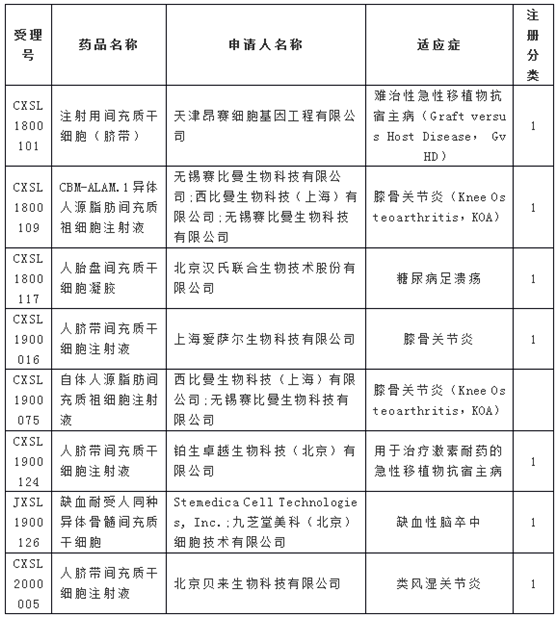
中國2020年至今4款臨床獲批幹細胞療法
根據中國國家藥品監督管理局藥品審評中心的資料,中國國內又一款間充質幹細胞新藥申請獲得臨床試驗默示許可,適應症為難治性移植物抗宿主病。這是2020年國內獲得臨床批件的第4款幹細胞新藥申請。截止目前,中國已經有8款間充質幹細胞新藥申請獲得臨床批件,適應症急性移植物抗宿主病、類風濕關節炎、缺血性腦卒中、膝骨關節炎、糖尿病足。
其中西比曼生物科技的CBM-ALAM.1異體人源脂肪間充質祖細胞注射液成為中國國內首個通用型基因幹細胞產品,且直接獲批II期臨床試驗。通用型幹細胞技術在臨床應用中有著重大意義。
目前,在全球範圍內,已經有16款幹細胞產品上市。